“초소형 단백질도 본다”⋯영남대 김동영 교수팀, 전자현미경 이용 ‘초소형 단백질 구조’ 규명


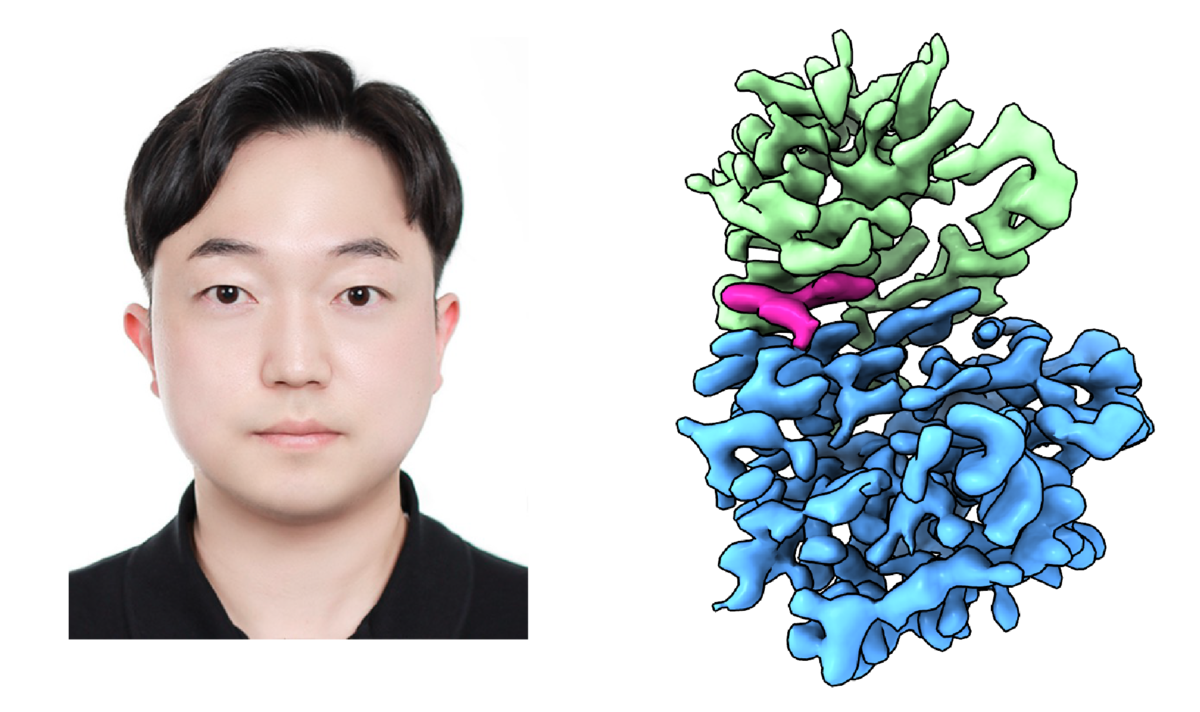
영남대학교 약학부 김동영 교수 연구팀이 기존 이론으로는 분석이 어려웠던 초소형 단백질 구조를 세계 최초로 규명하는 데 성공했다. 이번 성과는 초저온전자현미경(Cryo-EM)의 기술적 한계를 넘어 신약 개발 연구의 새로운 가능성을 제시한 것으로 평가된다.
연구팀은 그동안 구조 분석이 어려웠던 소형 단백질을 초저온전자현미경으로 정밀 분석하는 데 성공했다. 단백질은 인체 내에서 다양한 생리적 기능을 수행하는 핵심 물질로, 구조를 정확히 파악하는 것은 질병 원인 규명과 신약 개발의 출발점으로 여겨진다.
기존에는 강력한 X선을 활용하는 ‘X-선 결정학’이 단백질 구조 분석의 표준 기법으로 활용돼 왔다. 그러나 단백질을 결정 형태로 만들어야 하는 과정에서 실험적 제약이 크고 시간과 비용이 많이 든다는 한계가 있었다. 이를 보완하기 위해 등장한 초저온전자현미경은 시료를 급속 냉각한 뒤 이미지를 수집해 구조를 분석하는 방식으로, 최근 해상도 개선과 함께 핵심 분석 기술로 자리잡았다.
다만 초저온전자현미경은 일반적으로 분자량 200kDa 이상의 큰 단백질 분석에 적합하고, 소형 단백질의 경우 구조 규명이 어렵다는 것이 학계의 통설이었다. 2017년 노벨화학상 수상자인 리처드 헨더슨이 제시한 이론에 따르면 분석 가능한 최소 크기는 약 38kDa 수준으로 여겨져 왔다.
이번 연구에서 김 교수팀은 이러한 한계를 뛰어넘었다. 연구팀은 약 41kDa 크기의 말토스결합단백질 구조를 2.4Å 해상도로 규명했으며, 나아가 약 32kDa 크기의 단백질(PLK1)에 항암제 온반서팁이 결합한 구조를 3.4Å 해상도로 밝혀냈다. 이는 기존 이론적 한계보다 작은 단백질에서도 구조 분석이 가능함을 입증한 사례다.
특히 이번 연구는 단순 구조 규명에 그치지 않고, 소형 단백질과 약물 간 결합 상태까지 정밀하게 확인했다는 점에서 의미가 크다. 이를 통해 초저온전자현미경이 신약 개발 과정에서 약물 작용 메커니즘을 분석하는 핵심 도구로 활용될 가능성이 한층 높아졌다.
김동영 교수는 “현재 상용화된 장비만으로도 이론적 한계를 넘어서는 분석이 가능하다는 점을 보여줬다”며 “약물 결합 상태까지 확인할 수 있어 초저온전자현미경의 응용 범위를 크게 확장한 연구”라고 밝혔다. 이어 “장비 발전뿐 아니라 이를 활용할 수 있는 전문 인력 양성도 중요하다”고 강조했다.
이번 연구는 신약 개발 플랫폼 기업 바오밥에이바이오와의 공동연구로 진행됐으며, 해당 기업의 초저온전자현미경 장비를 활용했다. 논문 초안은 사전 공개 당시부터 국제 학계의 주목을 받았으며, 최종 연구 결과는 지난 4월 국제 학술지 네이처 커뮤니케이션즈 온라인판에 게재됐다.
/김락현기자 kimrh@kbmaeil.com