“우울증 약, 왜 이렇게 늦게 듣나 했더니”⋯ DGIST, 뇌 속 ‘신경펩타이드’가 해답 제시


항우울제를 복용하면 뇌 속 세로토닌 농도는 빠르게 증가하지만, 정작 환자가 기분 개선을 체감하기까지는 수주에서 수개월이 걸린다. 그동안 학계에서는 이를 두고 뇌 신경회로의 구조적 변화 때문일 것이라는 추정만 제기돼 왔다.
이 같은 ‘치료 지연’ 현상의 분자적 원인이 국내 연구진에 의해 세계 최초로 규명됐다.
DGIST는 뇌과학과 오용석 교수 연구팀이 항우울제의 효과가 지연되는 핵심 원인이 뇌 속 ‘신경펩타이드’ 생성과 회로 재건 과정에 있음을 밝혀냈다고 26일 밝혔다. 이번 연구 결과는 분자정신의학 분야의 세계적 학술지 Molecular Psychiatry에 게재됐다.
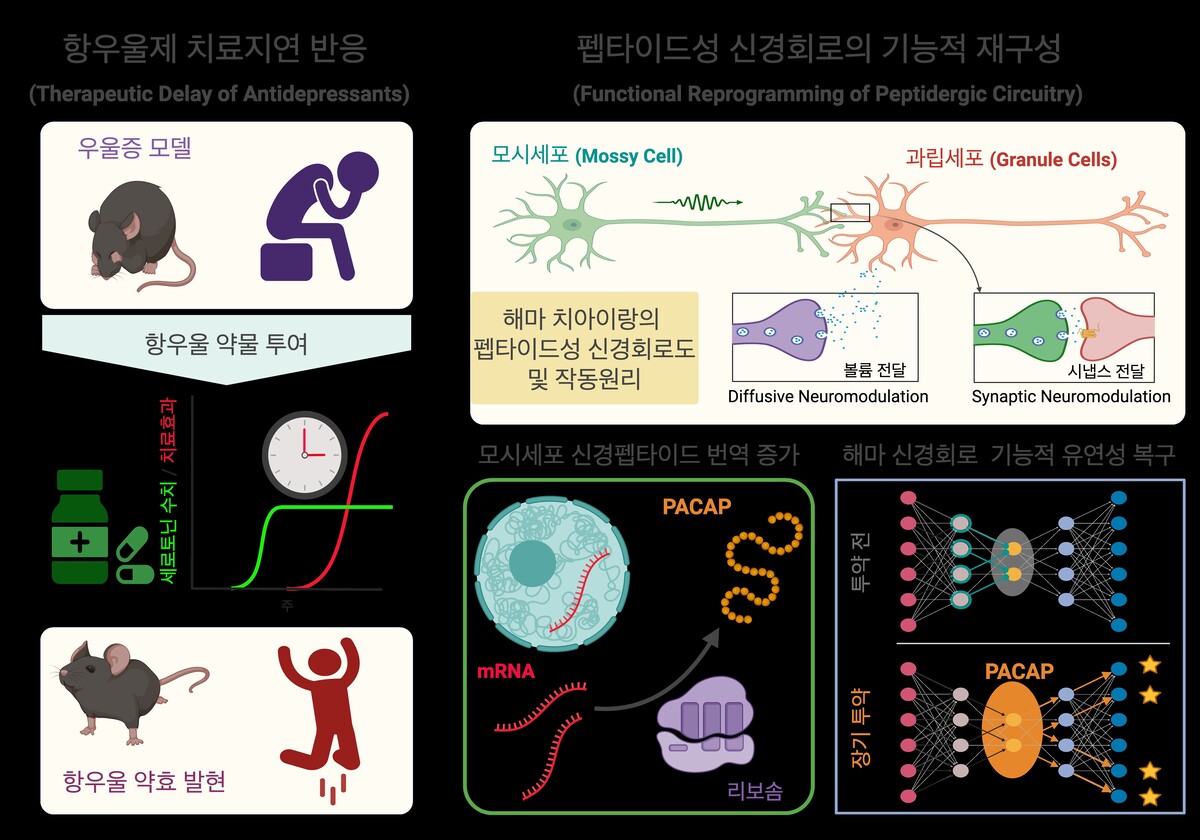
연구팀은 최신 유전체 분석 기술을 활용해 항우울제를 장기간 투여한 생쥐의 뇌 변화를 정밀 추적했다. 그 결과, 해마(hippocampus)에 위치한 ‘모시세포(Mossy Cell)’가 항우울제 자극을 받으면 특정 유전자의 단백질 번역을 가속화하고, 그 과정에서 신경펩타이드인 PACAP를 생성한다는 사실을 확인했다.
기존 선택적 세로토닌 재흡수 억제제(SSRI)는 복용 직후 세로토닌 농도를 높이지만, 연구팀에 따르면 이는 치료의 ‘시작 신호’에 불과하다. 실제 항우울 효과는 뇌가 신경펩타이드를 충분히 생산하고, 이를 통해 주변 신경세포와의 연결을 재구성하는 ‘회로 재프로그래밍’ 과정을 거친 뒤에야 나타난다는 것이다.
연구팀은 이 과정을 펩타이드 신경회로의 ‘번역 재편성(Translational Reprogramming)’이라고 명명했다. 즉, 세로토닌이 촉발한 신호가 단백질 번역 체계를 재편하고, 그 결과 생성된 신경펩타이드가 신경망을 다시 짜면서 비로소 치료 효과가 발현된다는 설명이다.
특히 이번 연구는 PACAP 기반 항우울 메커니즘이 암컷 생쥐에서 더욱 강하게 나타난다는 점도 규명했다. 이는 남녀 간 우울증 발병 기전과 치료 반응 차이를 설명할 수 있는 과학적 단서를 제시한 것으로, 향후 여성 환자 맞춤형 정밀의료 전략 개발에도 기여할 것으로 기대된다.
오용석 교수는 “우울증 치료 효과가 늦게 나타나는 이유를 신경펩타이드 생성 효율이라는 새로운 관점에서 설명했다”며 “앞으로는 세로토닌 조절을 넘어, 신경펩타이드의 생성과 성숙 과정을 직접 제어함으로써 복용 직후 효과를 기대할 수 있는 차세대 속효성 항우울제 개발로 연구를 확장할 계획”이라고 밝혔다.
이번 연구는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업 및 창의도전연구기반지원사업의 지원을 받아 수행됐다.
/김락현기자 kimrh@kbmaeil.com