중대 사항만 사전허가···기술혁신 대응 속도 낸다
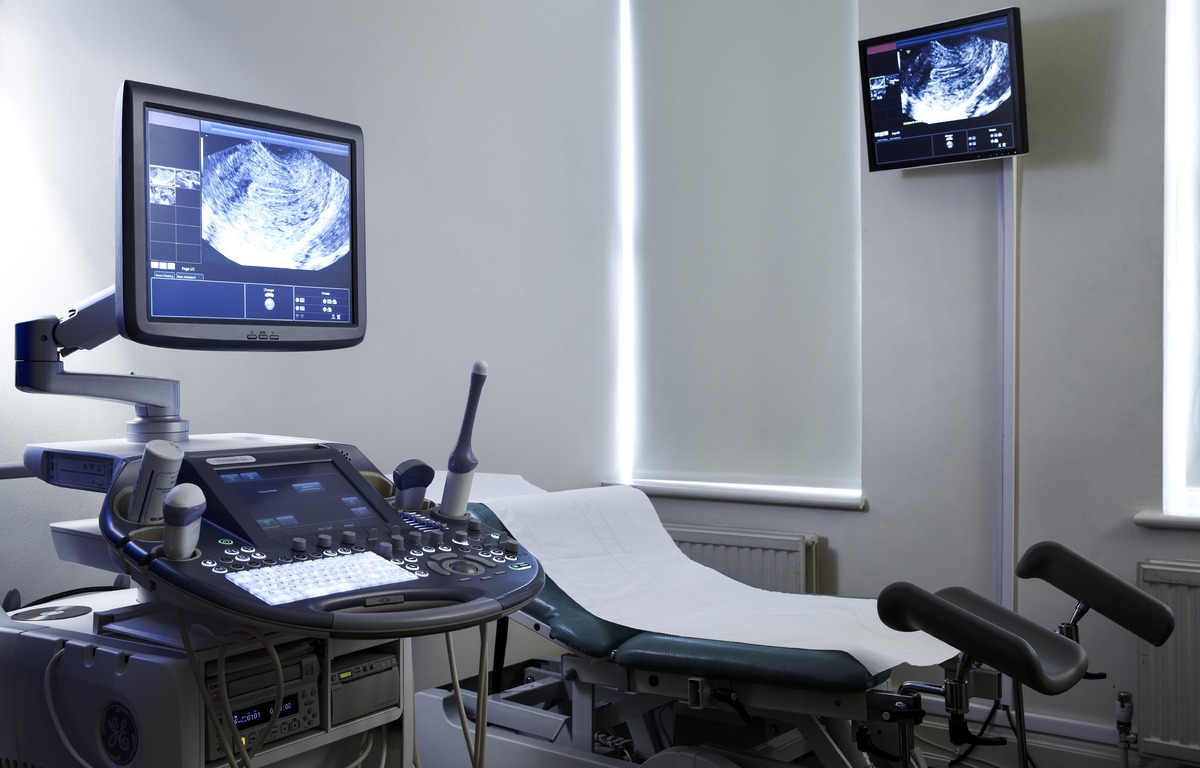
식품의약품안전처가 의료기기 변경허가 제도를 ‘네거티브 방식’으로 전환해 산업의 기술혁신에 신속 대응하기로 했다.
식약처는 3일 의료기기 중대 변경사항 외에는 업체가 자율적으로 변경·관리하도록 하는 내용을 담은 ‘의료기기법 시행규칙’ 개정안을 입법예고했다고 밝혔다. 입법예고 기간은 3월 3일부터 4월 13일까지다.
이번 개정안의 핵심은 의료기기 변경허가 네거티브 제도 도입이다. 안전성·유효성에 중대한 영향을 미치는 변경사항에 한해서만 사전 변경허가를 받도록 하고, 그 외 사항은 업체가 자체 평가·관리 절차에 따라 기록·관리하도록 제도를 개편한다. 중대 변경사항에는 소재지 변경(추가), 사용목적, 작용원리, 원재료 변경 등이 포함된다.
이에 따라 업체는 최초 허가 신청 시 변경 자체평가·관리 절차를 수립해 제출해야 하며, 이후 변경사항을 해당 절차에 따라 관리하게 된다. 정부 규제는 핵심 안전사항에 집중하고, 기업의 자율성과 책임은 확대하는 구조다.
조건부 허가사항 이행 확인기간도 단축된다. 제조 및 품질관리기준(GMP)을 일정 기간 내 갖출 것을 조건으로 허가를 받은 경우, 조건 이행 여부 확인 처리기간을 기존 20일에서 10일로 줄인다. 이를 통해 기업의 생산 준비와 제품 출시 일정이 보다 원활해질 전망이다.
아울러 의료기기 판매·임대업 직권말소 절차를 구체화하고, 유통 제품 수거검사 시 허가받은 시험규격에 부적합한 경우도 회수 대상에 포함하도록 회수 기준을 명확히 했다. 의료기기에서 이물이 발견됐을 때 조사 결과를 공표하는 권한도 지방식품의약품안전청장으로 정비해 행정의 신속성과 일관성을 높였다.
식약처는 “이번 개정은 의료기기 산업의 혁신을 지원하는 동시에 안전관리 체계를 합리적으로 정비하는 조치”라며 “산업 발전과 국민 안전이 조화를 이루는 방향으로 제도를 지속 개선하겠다”고 밝혔다.
/김진홍기자 kjh25@kbmaeil.com